Herausforderungen Praxis
Medizintechnik und Pharma, Chemie und Lebensmittel, in Ihrer Branche unterliegen Sie unterschiedlichen Regularien und Guidelines. Richtlinien im GxP-Umfeld werden beispielsweise von der Europäischen Arzneimittelagentur und der amerikanischen Food and Drug Administration (FDA), festgelegt. Die Einhaltung der festgelegten Richtlinien wird durch die Überwachungsbehörden der jeweiligen Länder regelmäßig überprüft. Beim Einsatz Ihres ERP-Systems und natürlich Ihrer QS- /QM-Lösung müssen alle Prozesse unter Berücksichtigung dieser regulatorischen Anforderungen gestaltet werden. Dies betrifft insbesondere die Anforderungen ISO13485 2016 EN und die Regularien 21 CFR Part 11. Gängige Verfahren zur Validierung von Software sind auf Grund ihrer Komplexität, des Aufwands, der Menge an Papier, dem fehlenden praktischen Nutzen etc. in der Regel eine erhebliche Belastung. Aus diesem Grund scheuen insbesondere mittelständige und kleine Firmen die dringend erforderliche Einführung von validierungspflichtiger Software.
Lösung QS1
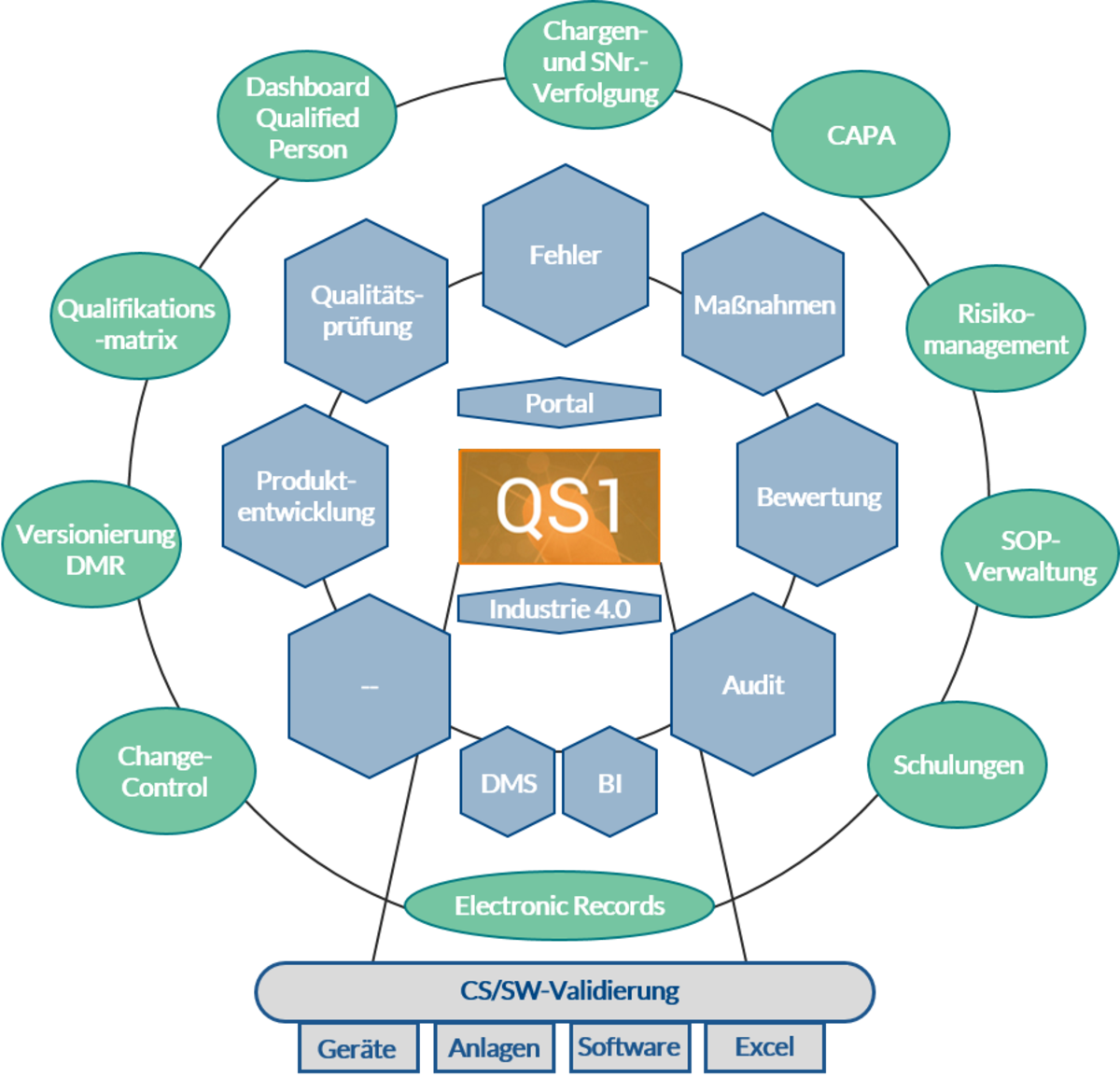
In der GxP-Branchenlösung bietet Ihnen QS1 beginnend mit der Produktentwicklung bis hin zum CAPA-Management eine Vielzahl von Modulen/Funktionen, welche es Ihnen erlauben, diese Abläufe effizient und normengerecht zu gestalten.
Wir unterstützen Sie nicht nur bei der eigentlichen Systemeinführung, sondern auch im Kontext Software-Validierung und Auditvorbereitung mit Bezug auf QS1 und Ihrem ERP-System.
- Qualifikationsmatrix:
Verwaltung und urkundlicher Nachweis von Qualifikationen Ihrer Mitarbeiter als Grundlage der BDE-Rückmeldungen sowie diverser Berechtigungen für Transaktionen. - CAPA-Management:
Vorkonfiguriertes Prozessmodul zum Management von CAPA, integriert mit den Reklamationsabläufen Kunden/Behörden und dem Maßnahmenmanagement von QS1. - Chargen-Verfolgung:
Interaktives Chargennetz zur durchgängigen Rück- und Nachverfolgung vom Rohmaterial bis zur Lieferung des Endproduktes für Chargen und Seriennummern mit integrierten Analyse- und Statistikfunktionen zur Ursachen-Analyse. - DashBoard-Qualified Person:
Leitstand für die verantwortliche Person zur Beurteilung der Konformität und Freigabe (auch automatisiert) von Chargen. - Elektronische Signaturen und Workflows für DMR-Daten:
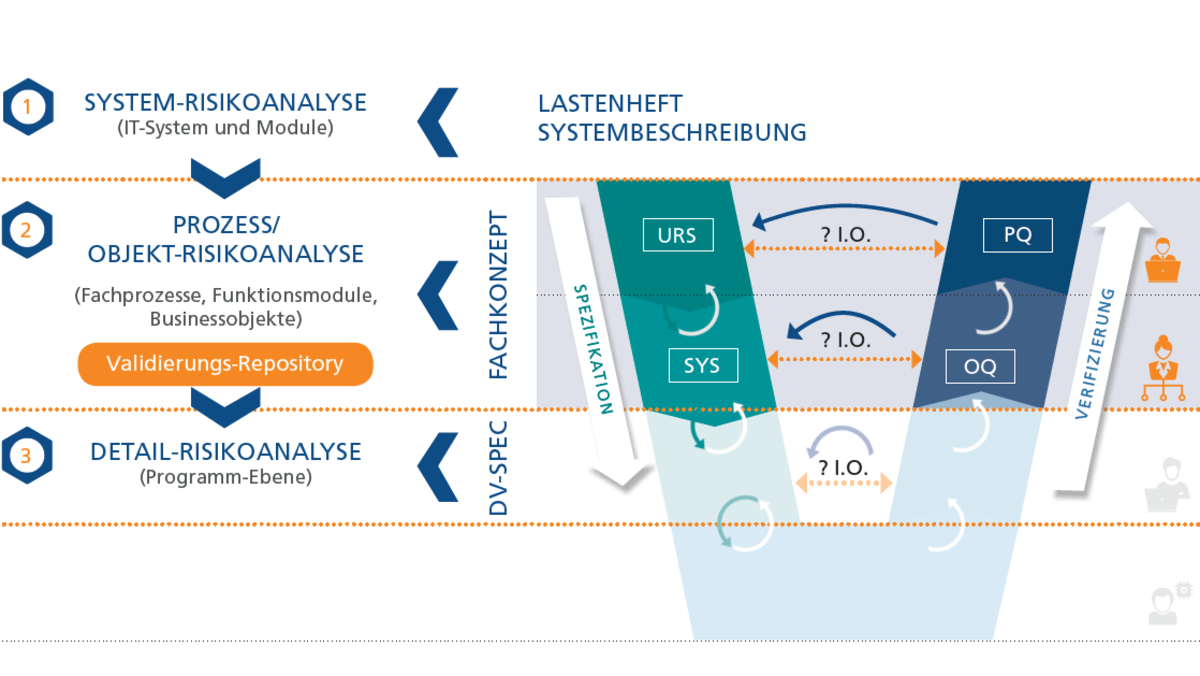
Versionierung von DMR-Daten wie z.B. Teilespezifikationen und Prüfpläne mit workflowbasierten Prüfungs- und Freigabeabläufen sowie zugehörigem Audit-Trail. - Anwendungssoftwarevalidierung (angelehnt an GAMP5):
Erfolgsfaktoren unserer Methodik zur Validierung der Anwendungssoftware QS1 / ERP